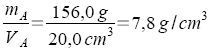 |
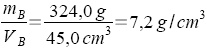 |
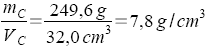 |
| 3 | Ausgewählte Begriffe der Physik |
| 3.1 | Dichte |
| 3.1.1 | Grundlagen |
|
Aufgabe: |
Von drei Körpern A, B und C bestehen zwei aus gleichem Material, einer aus einem anderen:
| Massen | mA = 156,0 g | mB = 324,0 g | mC = 249,6 g |
| Volumina | VA = 20,0 cm3 | VB = 45,0 cm3 | VC = 32,0 cm3 |
|
Rechengang und Überlegung |
Ein Vergleich ist möglich, wenn die Masse von jeweils 1cm3 bekannt ist.
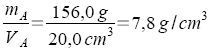 |
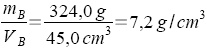 |
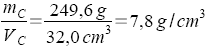 |
Der Quotient m/V hat bei den Körpern A und C denselben Zahlenwert.
Die Körper A und C bestehen aus demselben Material.
|
5
|
Der Quotient aus Masse und Volumen eines Stoffes heißt seine Dichte.
|
Die Dichte ist eine für den betreffenden Stoff spezifische, d. h. arteigene Größe. Von den Einheiten der Masse und des Volumens werden dezimale Vielfache und Teile gebildet (vgl. 1.1.4). Als besonderer Name für 1000kg ist die Tonne (1t), für 1dm3 das Liter (1l) gesetzlich.
Damit ergeben sich als Einheiten (Einheitenzeichen) für die Dichte:
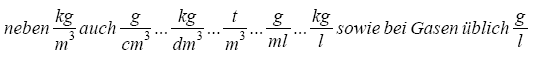
In der Praxis anschaulich, beim Rechnen einfach!
Da Volumina von Stoffen temperaturabhängig sind (vgl. 6.2.2 und 6.3), müssen auch Dichteangaben die jeweilige Bestimmungstemperatur tragen. Beispielweise bedeutet
|
|
Die Dichte von 10%iger Schwefelsäure, gemessen bei 20°C, beträgt 1,066 g/ml. |
Als Kurz-Symbol üblich: z. B.
![]() für Dichte bei 20 °C.
für Dichte bei 20 °C.
Dichtewerte, die bei anderen Temperaturen, z. B. 15 °C, gemessen wurden, können auf die jeweiligen Dichte bei 20 °C umgerechnet werden, wenn der Volumenausdehnungskoeffizient des betreffenden Stoffes bekannt ist (s. 6.2.2). Die Druckabhängigkeit des Volumens kann bei Feststoffen und Flüssigkeiten vernachlässigt werden, nicht jedoch bei Gasen (s. 6.3.2 und 6.3.3). Bei Gasen gibt man meistens die "Normdichte" an, die Dichte bei Normtemperatur und Normdruck (0 °C, 1013,25 hPa).