|
|
... | ||||||
| 1,045 | |||||||
| ↑ | ↓ | ||||||
| a | = | 0,005 | 1,047 | ||||
| ↓ | b | = | 0,003 | ||||
| 1,050 | |||||||
| ↑ | ... |
| 5.1.2.6 | Aufsuchen von Massenanteil- und Dichtewerten in Tabellen - Interpolieren |
Für die Berechnung der folgenden Aufgaben ist die Kenntnis der Dichte der Lösung erforderlich. Zueinander gehörende Werte von Dichte und Massenanteil sind in Tabellenwerken angeführt. Nicht tabellierte Zwischenwerte müssen interpoliert werden.
Auszug aus Dichte/Massenanteil-Tabellen wäßriger Lösungen:
| Dichte in g/ml |
HCl aq w in % |
H2SO4 w in % |
NaOH aq w in % |
| ... | ... | ... | ... |
| 1,035 | 7,464 | 5,493 | 3,29 |
| 1,040 | 8,490 | 6,237 | 3,75 |
| 1,045 | 9,510 | 6,956 | 4,20 |
| 1,050 | 10,52 | 7,704 | 4,66 |
| 1,055 | 11,52 | 8,415 | 5,11 |
| 1,060 | 12,51 | 9,129 | 5,56 |
| 1,065 | 13,50 | 9,843 | 6,02 |
| 1,070 | 14,50 | 10,56 | 6,47 |
| ... | ... | ... | ... |
|
Aufgabe 1: |
Berechne den Massenanteil von HCl in Salzsäure der Dichte ρ(HCl aq, 20°C) = 1,047 g/ml.
|
Rechengang: |
Der Wert ρ(HCl aq, 20°C) = 1,047 g/ml ist in der Tabelle nicht angeführt. Er liegt zwischen den Werten 1,045 g/ml und 1,050 g/ml. Demnach liegt auch der gesuchte Massenanteil zwischen den entsprechenden Werten 9,510% und 10,52%.
Es muß interpoliert, der gesuchte Zwischenwert über eine Proportion berechnet werden:
Die Differenzen
aus a den angesprochenen tabellierten Dichte-Werten
und b dem Dichte-Wert der Aufgabe und dem nächsthöheren Tabellenwert
stehen im gleichen Verhältnis wie
die Differenzen
aus c den angesprochenen tabellierten Massenanteilen
und d dem gesuchten Massenanteil und dem nächsthöheren Tabellenwert.
|
|
... | ||||||
| 1,045 | |||||||
| ↑ | ↓ | ||||||
| a | = | 0,005 | 1,047 | ||||
| ↓ | b | = | 0,003 | ||||
| 1,050 | |||||||
| ↑ | ... |
|
|
... | ||||||
| 9,510 | |||||||
| ↑ | ↓ | ||||||
| c | = | 1,01 | x | ||||
| ↓ | d | = | ? | ||||
| 10,52 | |||||||
| ↑ | ... |
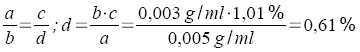
Wird der errechnete Wert d vom höheren Tabellenwert abgezogen, ergibt sich der gesuchte Massenanteil x zu 10,52% - 0,61% = 9,91%.
Salzsäure der Dichte ρ20 = 1,047 g/ml ist 9,91%ig.
|
Aufgabe 2: |
Welche Dichte hat 10,00%ige Schwefelsäure?
|
Rechengang: |
Der Massenanteil ist in der Tabelle nicht angeführt. Es muß interpoliert werden:
|
|
... | ||||||
| 9,843 | |||||||
| ↑ | ↓ | ||||||
| a | = | 0,717 | 10,00 | ||||
| ↓ | b | = | 0,56 | ||||
| 10,56 | |||||||
| ↑ | ... |
|
|
... | ||||||
| 1,065 | |||||||
| ↑ | ↓ | ||||||
| c | = | 0,005 | x | ||||
| ↓ | d | = | ? | ||||
| 1,070 | |||||||
| ↑ | ... |
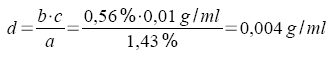
Mit dem errechneten Wert d ergibt sich die gesuchte Dichte x zu 1,07 g/ml - 0,004 g/ml = 1,066 g/ml.
10,00%ige Schwefelsäure hat die Dichte ρ20 = 1,066 g/ml.