| 11.5.2 | Berechnen von Brennwert und Heizwert fester und flüssiger Brennstoffe |
|
Aufgabe: |
Berechne
a) den spezifischen Heizwert
b) den spezifischen Brennwert von Benzol C6H6.
Molarer Heizwert Hu, m einiger Brennstoffe
| kJ / mol | kJ / mol | ||
| Ethan | 1432 | Methan | 804 |
| Ethanol | 1696 | Propan | 1834 |
| Benzol | 3140 | Wasserstoff | 243 |
| Kohlenoxid | 285 | Toluol | 3684 |
|
Rechengang: |
a) Umrechnen des molaren Heizwertes Hu, m in den spezifischen Heizwert Hu:
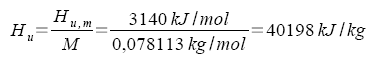
Der spezifische Heizwert Hu(C6H6) = 40198 kJ/kg
b) Für 1 kg Benzol gilt:
Nach C6H6 + 7,5 O2 → 6 CO2 + 3 H2O entstehen bei der Verbrennung von
| 1 mol C6H6 = 78,113 g C6H6 | 3 mol H2O - Dampf = 54,0456 g H2O - Dampf |
| aus 1000 g C6H6 | x H2O - Dampf |
| x = 692 g |
Von dieser Wassermasse betragen:
die Kondensationswärme
Q1 = m * r
= 0,692 kg * 2257 kJ/kg
= 1562 kJ
die Abkühlungswärme von 100 °C auf 25 °C
Q2 = m * c * ΔJ
= 0,692 kg * 4,187 kJ/kg * K * 75 K
= 217,3 kJ
ΔH von 1 kg Benzol ist damit:
Hu + Q1 + Q2
40199 kJ + 1562 kJ + 217 kJ = 41978 kJ
der spezifische Brennwert Ho (C6H6) = 41978 kJ/kg.