INDUKTIVITÄT UND MESOMERIE
während der Kohlenstoff, an dem der Substituent gebunden ist, partiell positiv geladen wird (Zeichen d+). Ist die Elektronegativität des Substituenten geringer als die des in der Einteilung als Nullpunkt definierten Wasserstoffs, so erzielt man einem +I-Effekt, und der betrachtete Substituent lädt sich positiv auf (Zeichen d+). Diese induktiven Effekte sind additiv und über meherere Atome hinweg vorhanden, wobei sie sich mit zunehmender Entfernung abschwächen. Gruppen mit -I-Effekt stabilisieren negative Ladungen im restlichen Teil des Moleküls. Gruppen mit +I-Effekt stabilisieren positive Ladungen im restlichen Teil des Moleküls. Bsp.: -I-Effekt des Chlors (ENCl = 3.2, ENC = 2.6): 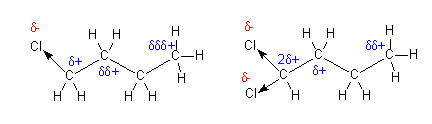 Induktive Effekte haben z.B. einen Einfluß auf die Stärke von Säuren oder auf die elektrophile Substitution an Aromaten: 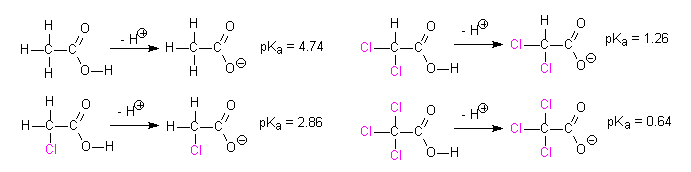 Die Verteilung von Elektronenladung (Delokalisierung) über mehrere Atome hinweg führt zu einer Stabilisierung, d.h. einer energetisch tieferen Lage des Moleküls. Diesem Phänomen begegnet man bei Molekülen, die sich durch mehrere Grenzformeln darstellen lassen. Bei den dargestellten fiktiven Grenzformeln (verbunden durch einen zweiköpfigen Pfeil) handelt es sich nicht um die wirkliche Elektronenverteilung, sondern die Elektronen sind gleichmäßig über den gesamten Raum verteilt, was durch punktierte Linien angedeutet werden kann (Resonanzhybride), z.B. das Carbonat-Ion, CO32-: 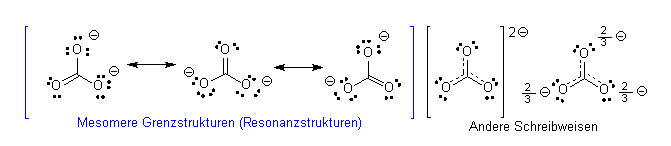 Bei den mesomeren Grenzstrukturen sind immer p- und Über s-Einfachbindungen kann keine Ladung verschoben werden, sonder nur ein induktiver Effekt (s.o.) wirken. Je mehr mesomere Grenzformeln sich zeichnen lassen, desto energieärmer ist das Molekül! Ein besonders wichtiger Fall von Delokalisierung durch Resonanzhybride liegt bei aromatischen Verbindungen vor. In der Reihe Cyclohexen, 1,3-Cyclohexadien und 1,3,5-Cyclohexatrien würde die Energie (hier: Hydrierungswärme) des 1,3,5-Cyclohexatrien viel höher liegen, wenn es nicht durch Resonanz stabilisiert wäre: 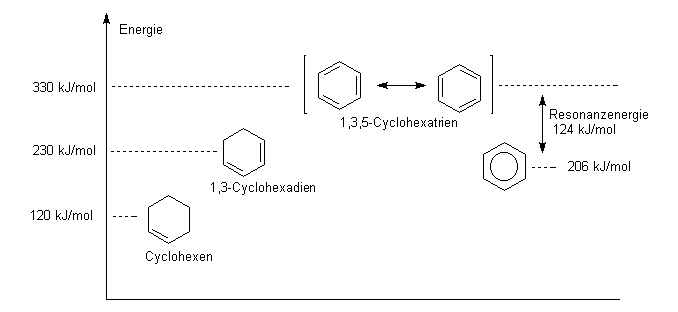
|